A maior lição da biotina é a importância das ligações H não clássicas nos complexos proteicos-ligantes.
O título vem do resumo de um artigo (cite) 10.1021/acs.jmedchem.1c00975 (/cite) analisando por que a biotina (vitamina B7) é um ligante tão forte e eficaz para proteínas, com uma energia livre de ligação (não covalente) que se aproximava de 21 kcal/mol. O autor argumenta que um acúmulo de CH-π e CH-O juntamente com ligações mais clássicas de hidrogênio e aumentado por uma ligação de hidrogênio centrada em enxofre, orifícios de oxianião e solvatação de água, responsável por essa grande energia de ligação.
Aqui, pensei em apresentar uma visualização dos arredores da biotina usando o método da análise NCI (não-covalente), que analisa o comportamento da densidade de elétrons na “fraca” (ou seja regiões não covalentes) da biotina. Isso fornece uma medida mais objetiva das interações importantes, independentemente do que podemos considerar importante em virtude de ter rótulos anexados (como por exemplo “Ligação de hidrogênio”).
- Comecei obtendo as coordenadas de Streptavidin (doi: 10.2210/pdb3ry2/pdb) uma proteína onde a biotina foi co-cristalizada. (CITE) 10.1107/S0907444911027806 (/cite)
- Carregado no Programa de Mercúrio do CCDC, selecionei a própria biotina da molécula e depois adicionei à seleção seus contatos próximos com vários grupos na proteína da estreptavidina. Essas adições foram truncadas e tapadas com um grupo metil para permitir uma função de onda para a montagem ser calculada.
- Os hidrogênios foram então adicionados a essa estrutura para completar as valências atômicas, usando posições “idealizadas” e garantindo que, quando os rotamers fossem possíveis, eles foram configurados para formar ligações de hidrogênio.
- Um cálculo (doi: 10.14469/hpc/9982 No ωB97XD/DEF2-TZVPP/SCRF = nível da água) foi realizado.
- Os atomos pesados coordenam (ou seja não hidrogênios) são inalterados da estrutura de raios-X. Como as posições do átomo medidas por difração de raios-X e calculadas usando um procedimento DFT são ligeiramente diferentes, as coordenadas originais também foram submetidas a três ciclos de otimização de geometria baseada em DFT (doi: 10.14469/hpc/9983) para refletir melhor a densidade de elétrons na molécula.
- As funções de ondas resultantes na forma de um .fchk Arquivo (para geometrias não optimizadas e parcialmente otimizadas) foram usadas para calcular uma grade de pontos de densidade de elétrons totais
- A densidade, na forma de um cubo de pontos, foi alimentada com JMOL usando os comandos
carregar biotin_den.cub; Parâmetros ISoSurface (0,5 1 0,0005 0,05 0,95 1,00) NCI ""; Coloration IsoSurface "BGGYOR" Faixa -0,04 0,04;
e a superfície da NCI resultante foi escrita usando o comando Escreva biotin.jvxl para inclusão aqui. - Este é o gráfico da NCI obtido das coordenadas brutas do arquivo PDB.
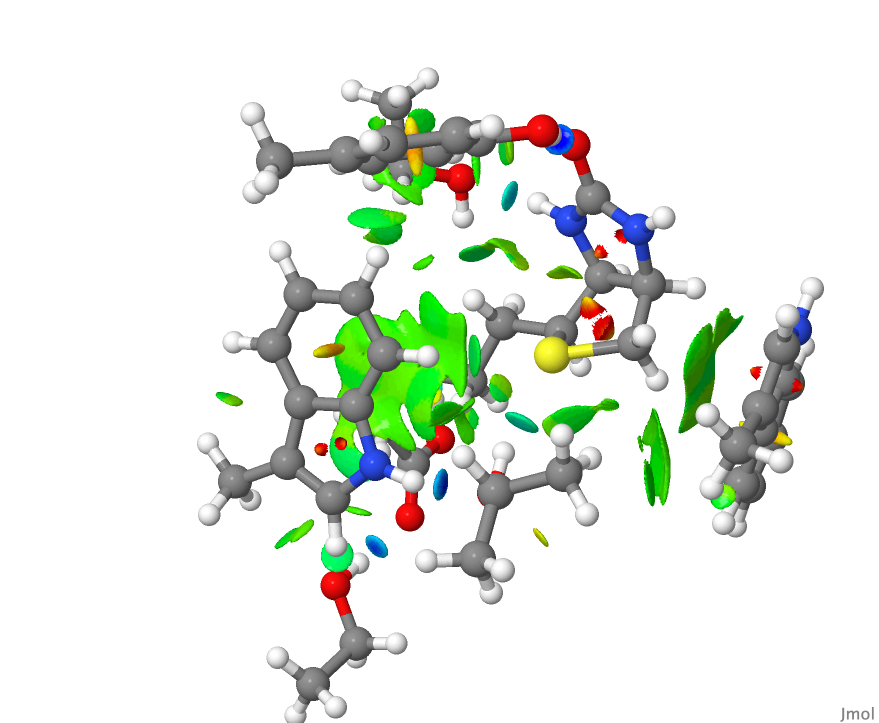
- Este é o gráfico da NCI obtido das coordenadas do arquivo PDB após três ciclos de otimização de geometria. Você pode identificar alguma diferença?
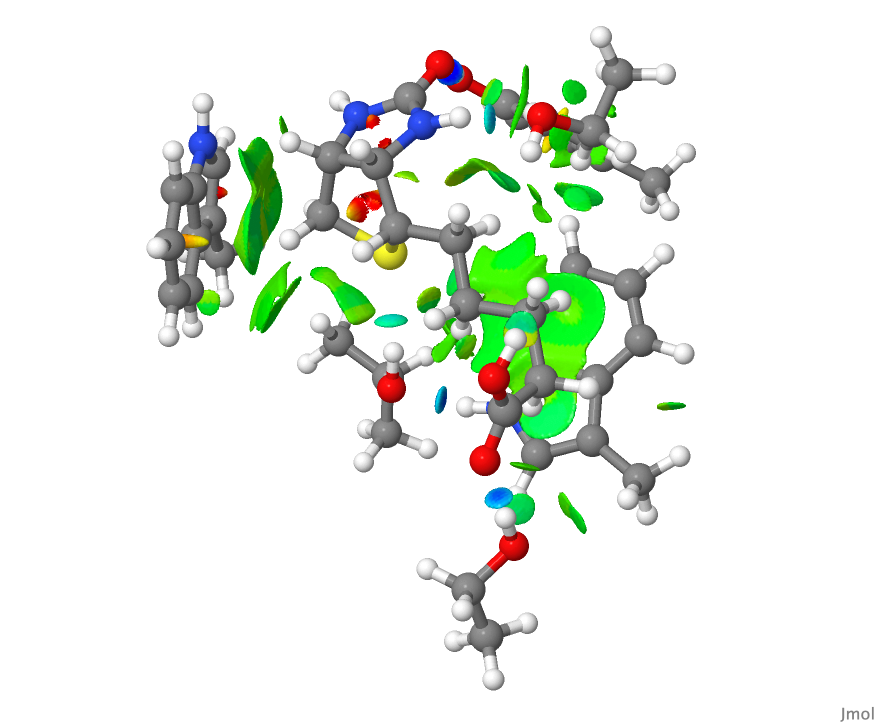
- Agora, esses modelos estão disponíveis para você explorar clicando nas imagens acima.
- As regiões azuis representam ligações de hidrogênio “fortes” ou clássicas. Existem quatro deles nos diagramas NCI acima e todos são compactos, outra característica de fortes ligações de hidrogênio.
- A ligação de hidrogênio ao enxofre é um pouco mais fraca e aparece na tela como uma superfície compacta, embora agora de cor ciana.
- As regiões restantes são difusas e verdes e representam “interações” mais fracas. Eles são menos compactos que as ligações clássicas de hidrogênio. Eles não representam um vínculo tanto como uma região atraente na molécula e, portanto, o termo não clássico. A maioria são grupos CH próximos à superfície π de um anel aromático, mas alguns também são interações ch … o.
Vá em frente e carregue a superfície 3D. Você deve explorar particularmente as regiões CH-π e observar que elas não estão necessariamente associadas a uma ligação CH específica, mas com várias delas combinando para formar uma interação com uma região π aromática.
O que pode surgir é a percepção de que as interações de ligação nem sempre estão entre átomos específicos, como nas “ligações” de hidrogênio clássico, mas também constituem “regiões estabilizadoras” entre o ligante e a proteína. Você provavelmente identificará várias dessas regiões que não estão realmente listadas no próprio artigo. (CITE) 10.1021/acs.jmedchem.1c00975 (/cite) Eu sugiro que não nos referamos a ligações ch … π, como no título citado deste put up, mas como como como como CH… π Regiões.
Seria ótimo se todo o complexo pudesse ser submetido a uma análise NCI. As funções de onda para> 2000 átomos podem ser obtidas atualmente, mas exigiria um pouco de trabalho para garantir que a densidade possa ser calculada com precisão o suficiente e com resolução cúbica alta o suficiente para ser útil no contexto da análise do NCI.
Este weblog tem doi: 10.14469/hpc/9984
Relacionado
Esta entrada foi publicada no sábado, 27 de novembro de 2021 às 10:32 e é arquivada em Química interessante. Você pode seguir qualquer resistência a esta entrada através do RSS 2.0 alimentar. Você pode Deixe uma respostaou trackback do seu próprio website.






