No publish anterior(1) Eu discuti a possibilidade de que uma forma de alta energia do dímero de óxido nítrico 1 No entanto, pode ser capaz de ser detectado usando armadilhas adequadas (como hidrogenação ou cicloadição). No entanto, uma alternativa interessante é que essa espécie pode ser presa pelo próprio óxido nítrico. De acordo com (2) Em um artigo intitulado “Decomposição de óxido nítrico a pressões elevadasA taxa desta reação Termolecular 3NO → N2O + não2 Dizem que obedecem à cinética de terceira ordem. Um mecanismo plausível para esse processo é mostrado abaixo.
Portanto, surge agora a questão sobre se esse processo sempre interviria para evitar qualquer captura de espécies 1. Hora de algumas energias calculadas.(3) A reação ocorre em duas etapas, TS1formando Intque então dá o produto by way of TS2. O IRC combinado para esses processos é mostrado abaixo,† e a barreira complete de energia de 1 + NÃO para esse processo é pequeno (~ 7 kcal/mol).
O comprimento da ligação nn ao longo do curso dessas duas etapas é mostrado abaixo,† Indicando que ele começa e termina com uma ligação ~ n≡N, conforme implícito no esquema acima.
A resposta do momento dipolo é mostrada abaixo.†
A animação para o IRC para TS1 é mostrada abaixo:
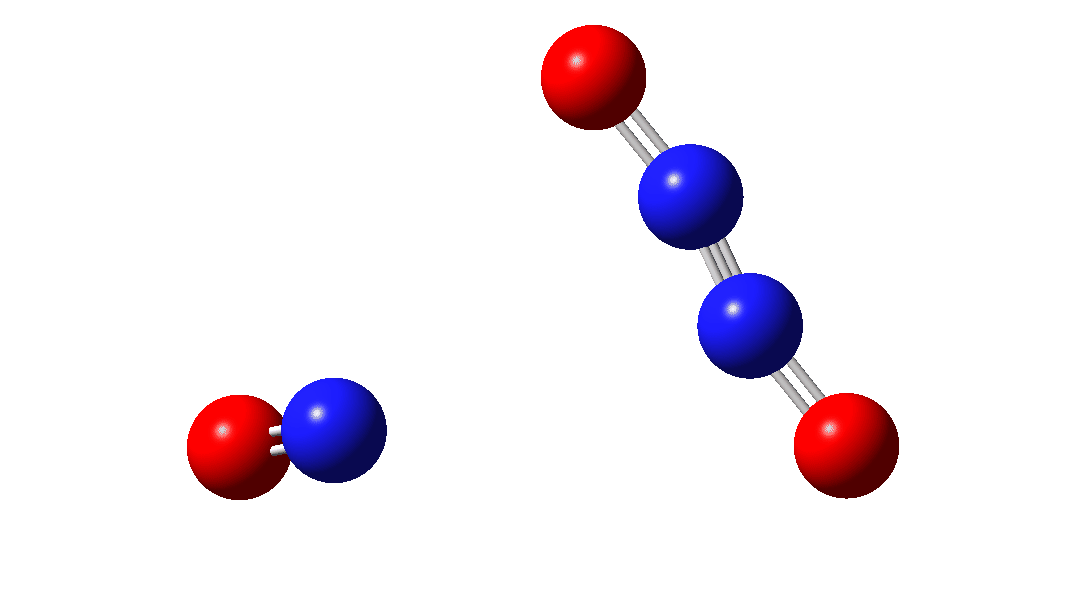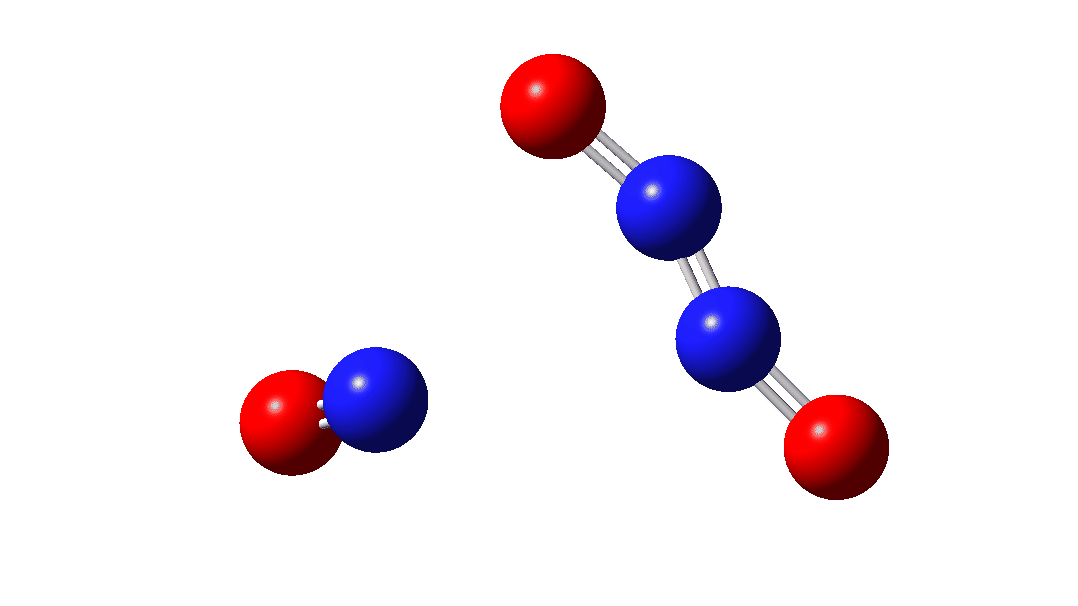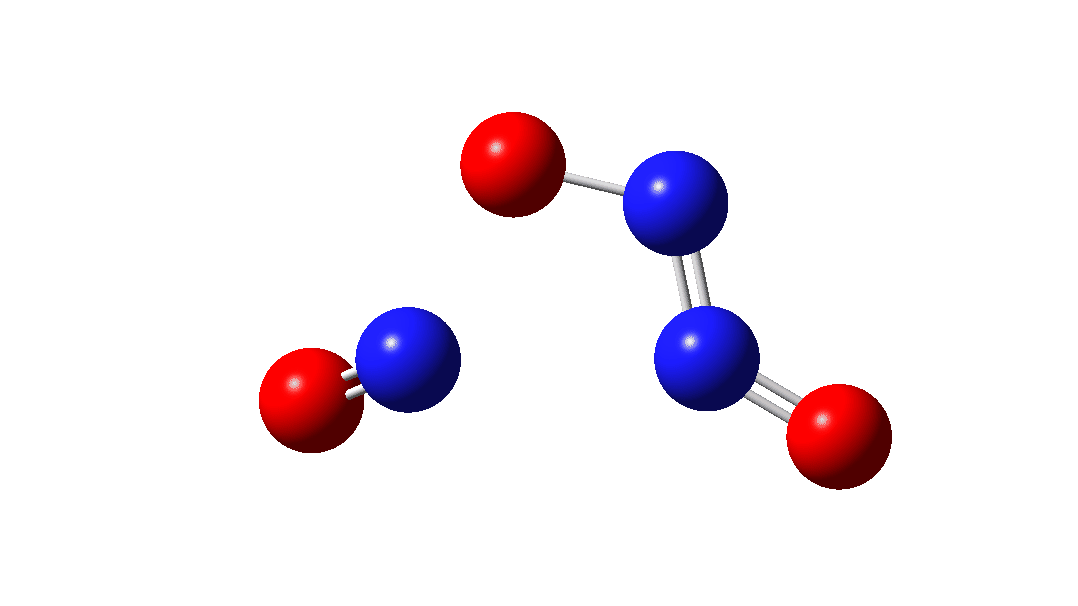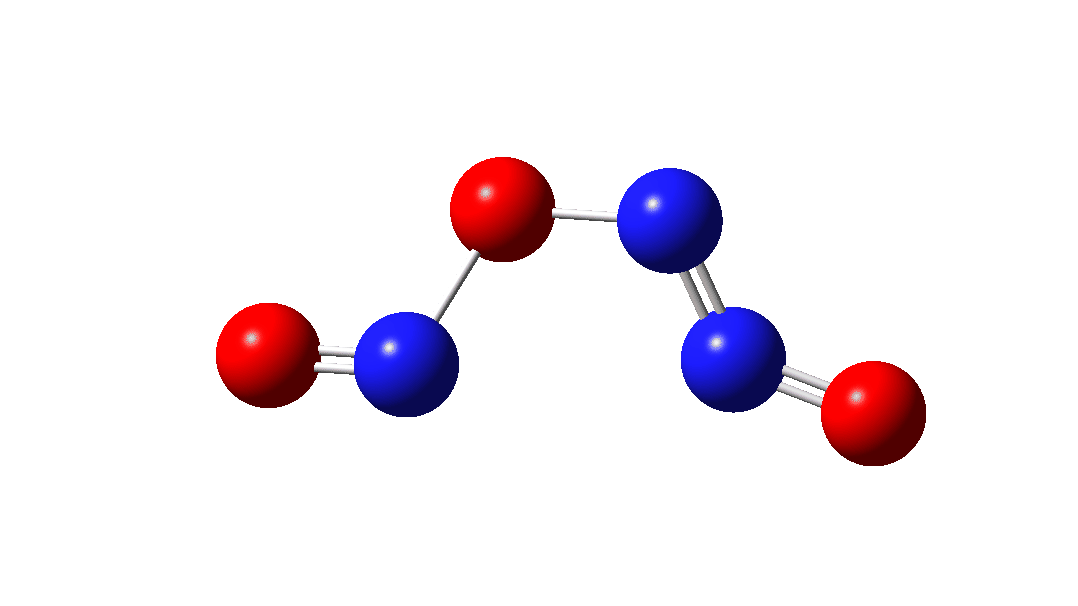
O intermediário, n3O3 tem uma densidade de rotação que cobre todos os seis átomos (clique na imagem abaixo para ver o modelo 3D interativo), por isso é difícil de representar por por exemplo uma única estrutura de ligação de valência, como mostrado acima.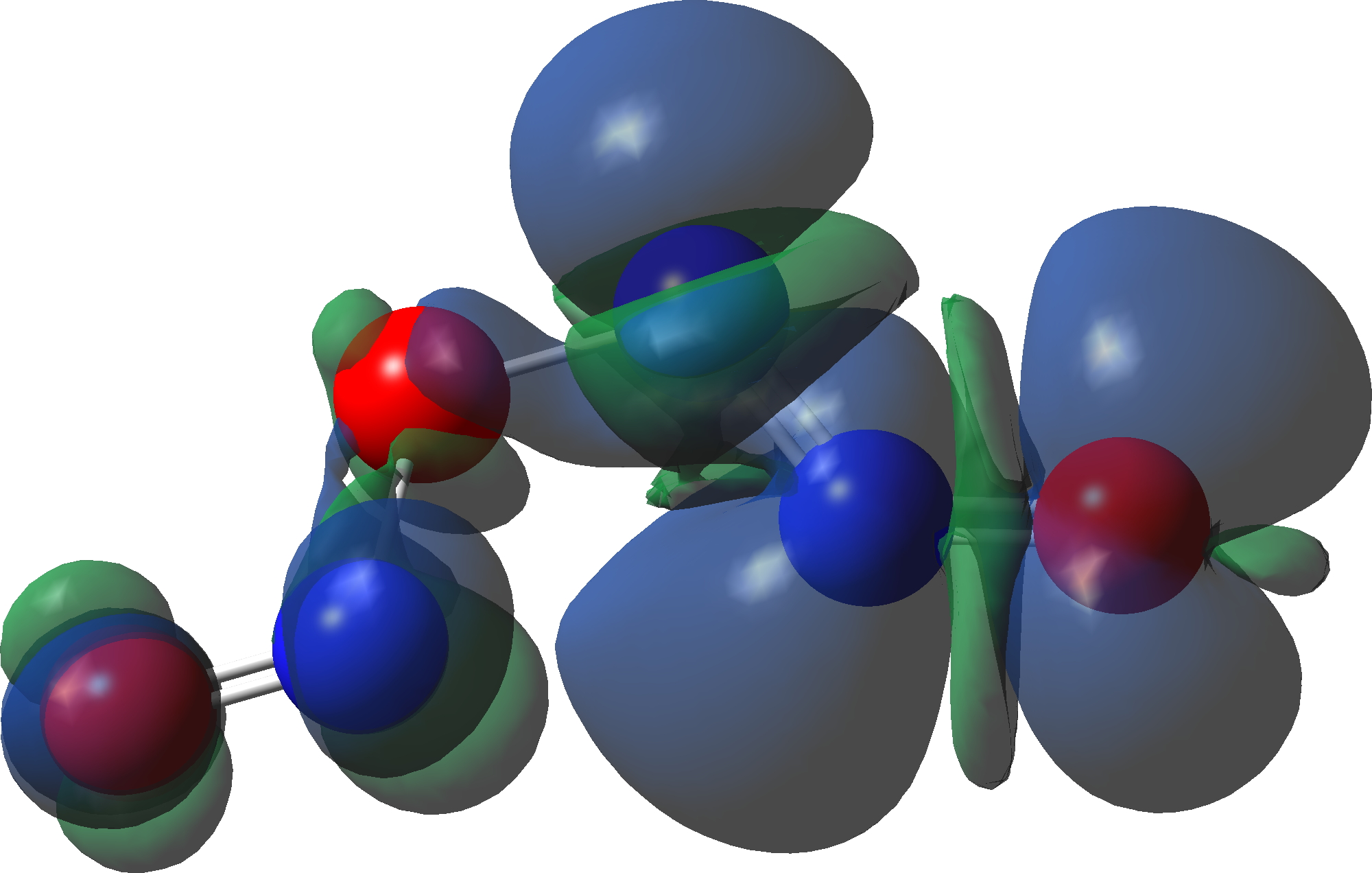
O IRC para TS2 está animado abaixo:
O alto valor para ΔG‡ ~ 39,5 kcal/mol surge em grande parte devido à perda de entropia na redução de três moléculas para uma nos estados de transição – e pode ser comparado com por exemplo O valor de ΔG‡ 31,0 kcal/mol citado anteriormente para a dimerização bimolecular de duas moléculas de NO.(4)
A história ainda não acabou, já que outras conformações para essa reação ainda estão sendo exploradas. Atualmente, parece que existe apenas uma pequena janela de energia livre entre a formação de espécies 1 e reagindo ainda mais da maneira 3No → N2O + não2 Como mostrado acima, parece improvável nesta fase que 1 pode ser facilmente detectado.
† A ligeira descontinuidade visível em ~ IRC +1 é devido a uma mudança conformacional entre o ponto remaining do IRC para TS1 e o ponto de partida para TS2.
Doi: 10.59350/rzepa.29665
Referências
- H. rzepa, “hidrogenando a ligação tripla Ntante ainda mais misteriosa em um dímero de óxido nítrico”., 2025. https://doi.org/10.59350/rzepa.29626
- T. Melia, “Decomposição de óxido nítrico a pressões elevadas”, Jornal de Química Inorgânica e Nuclearvol. 27, pp. 95-98, 1965. https://doi.org/10.1016/0022-1902(65)80196-8
- H. rzepa, “Reações alternativas da ligação tripla N≡N em um dímero de óxido nítrico”., 2025. https://doi.org/10.14469/hpc/15549
- H. rzepa, “A ligação tripla Ntante ainda mais misteriosa em um dímero de óxido nítrico”., 2025. https://doi.org/10.59350/rzepa.29429
Relacionado
Esta entrada foi publicada na quarta -feira, 3 de setembro, 2025 às 11h25 e é arquivada em Química interessante. Você pode seguir qualquer resistência a esta entrada através do RSS 2.0 alimentar. Você pode Deixe uma respostaou trackback do seu próprio web site.






