Durante o café do café no segundo dia dos 3rd Simpósio de Crick Beddington, eu me aproximei da Dra. Giulia Boezio, um pós -doutorado no Briscoe Lab no Francis Crick Institute. Como embriologista de Chick, eu já estava ciente de seu trabalho, mas fiquei intrigado ao saber mais sobre a técnica genômica de código de barras que ela adaptou para uso em nosso organismo modelo favorito!
O Briscoe Lab está interessado em como a enorme diversidade de subtipos neuronais surge na medula espinhal. Diferentes tipos de células se originam de diferentes posições ao longo do eixo dorsoventral, constituindo 11 domínios discretos de células progenitoras (Holguera e Desplan, 2018; Le Dréau e Martí, 2012; Sagner e Briscoe, 2019). Mas ainda não sabemos como esses tipos de células surgem-um tipo de neurônio maduro vem de um progenitor específico ou dois neurônios maduros diferentes compartilham um progenitor sem fim? Ou talvez os caminhos de diferenciação convergem – dois progenitores diferentes podem dar origem ao mesmo tipo de célula last. Giulia pretende esclarecer essas questões, que surpreendentemente não foram revisitadas há mais de 30 anos (Leber et al., 1990; Leber e Sanes, 1991).
A Giulia adaptou uma técnica de código de barras genômicas chamada Larry (Linhagem e RNA Recuperação; Weinreb et al., 2020) – originalmente desenvolvidas para células em cultura – para uso no embrião de pintinhos. A infecção viral é usada para fornecer códigos de barras na medula espinhal de pintinhos no estágio 12 (dia 2 do desenvolvimento). Cada código de barras é único e é expresso ao lado do GFP, permitindo que as células infectadas sejam rastreadas ao longo do tempo. Os embriões são incubados para se desenvolver por vários dias, antes que as células maduras sejam coletadas em um dos três momentos (estágio 28, 31 e 35). Eles são então classificados para obter as células que expressam GFP e perfiladas usando RNaseq de célula única. Após identificar qual cluster corresponde a qual tipo de célula, Giulia pode ver quais códigos de barras estão presentes em cada cluster. Como todas as células com o mesmo código de barras são derivadas de um único progenitor, isso permite que um histórico de linhagem retrospectivo seja montado. Eu me perguntei como eles podem garantir que cada código de barras seja completamente único, mas Giulia explicou: “Temos quase meio milhão de códigos de barras em nossa biblioteca. Isso normalmente não seria suficiente, se estivéssemos infectando muitas, muitas células.” Isso significa que an opportunity de infectar duas células independentes com o mesmo código de barras é extremamente pequena. Ela também verificou cinco embriões separados e não encontrou nenhuma sobreposição de código de barras – por isso é seguro assumir que, em um embrião, cada código de barras é único.
A partir dos dados de RNaseq de células únicas, ela descobriu que as células da medula espinhal se agrupam em cinco compartimentos de linhagem – o que significa que os progenitores contribuirão principalmente para as células em um desses cinco compartimentos de linhagem e raramente contribuirão para mais de um. Alguns tipos de células eram mais abundantes que outros – isso é particularmente verdadeiro para os neurônios DI4 e DI5 dorsal, que compõem mais da metade de todos os neurônios em toda a medula espinhal. Esses neurônios sensoriais estão envolvidos na sensação de toque e dor (Lai et al., 2016) e, apesar de sua abundância, não são muito bem estudados. Giulia observou que suas proporções mudaram com o tempo; No estágio 28, ela viu muito mais DI4 que os neurônios DI5, mas no estágio 31 isso equivalia a aproximadamente 50:50 – isso faz todo o sentido, já que um é um neurônio excitatório e o outro é um neurônio inibitório no mesmo circuito.
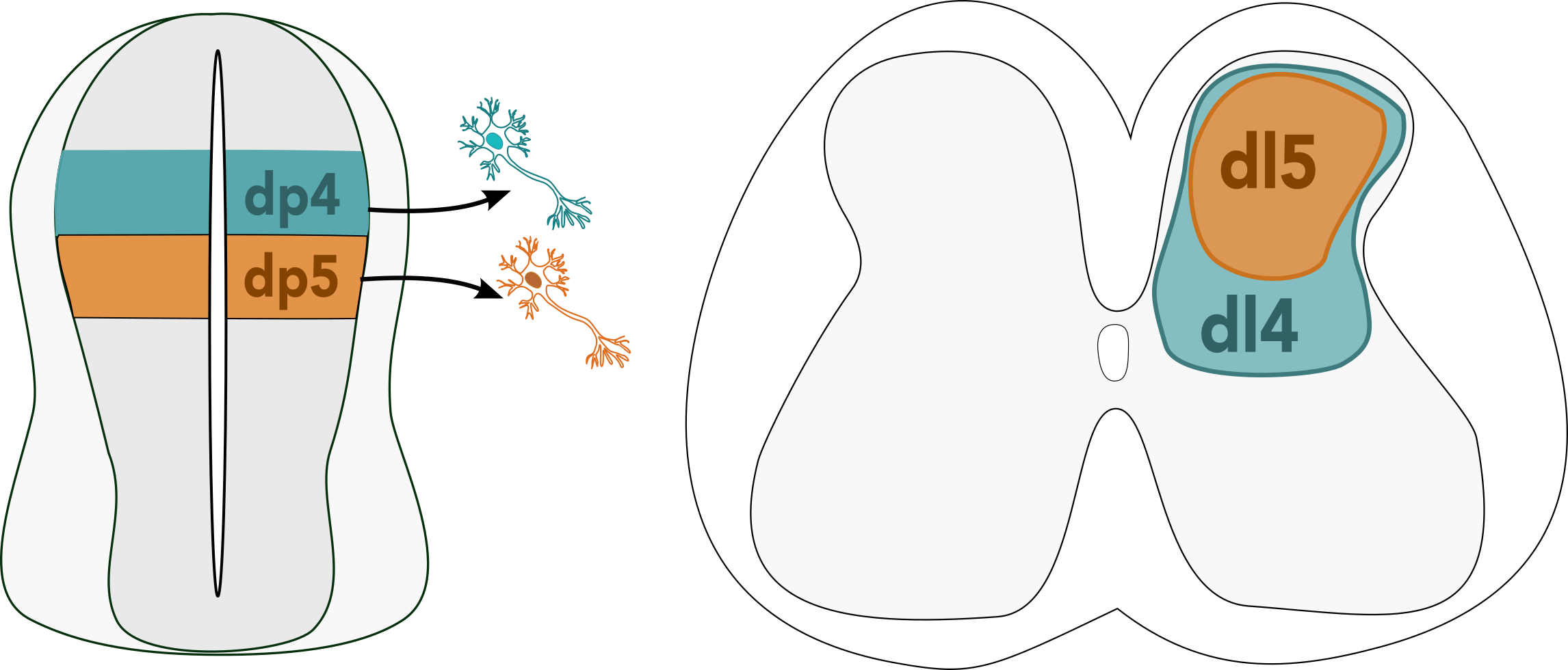
Mas como esse desequilíbrio surge e como se corrige mais tarde? “Initially, after I noticed this, I assumed that the best clarification can be that the blue (dI4) cells are born earlier, after which ultimately the orange (dI5) cells would catch up one way or the other. However we needed to dig a bit deeper into the clonal information, and this clarification did not appear to suit”, Giulia mentioned, after observing an preliminary peak of dI4 neurons, adopted by a peak in each dI4 and dI5 neurons later in growth. Acontece que em estágios anteriores, a maioria dos neurônios DI4 deriva de clones que produzem apenas neurônios DI4, enquanto nos estágios posteriores, a grande maioria dos clones produz uma proporção uniforme dos neurônios DI4 e DI5. Isso sugere que existem dois tipos de progenitoras diferentes – um que produz apenas neurônios DI4 e um que produz DI4 e DI5 em quantidades iguais. A Giulia está atualmente trabalhando para ajustar esses dados a diferentes modelos matemáticos para encontrar uma trajetória de diferenciação que possa explicar esse resultado.
Este sistema se aplica a outras espécies? Para descobrir, Giulia usou culturas ex vivo de fatias de tronco embrionárias humanas-uma técnica (que realmente soa como ficção científica para mim!), Na qual seções transversais da medula espinhal são cultivadas usando uma interface aérea-líquido, exposto ao meio de cultura de células do fundo e do ar de cima. O trabalho com embriões humanos é notoriamente difícil, pois você não pode controlar a disponibilidade, nem em que estágio estará disponível para trabalhar. Giulia conseguiu obter embriões humanos de 6 semanas de idade (CS17) – mais velha do que gostaria, mas decidiu seguir em frente com o experimento de qualquer maneira. Ela infectou as fatias de tronco CS17 com códigos de barras Larry e os cultivou por 7 dias, coletando e traçando as células da mesma maneira que para o experimento de pintinhos. Ela descobriu que o DI4 e o DI5 dominavam outros neurônios em termos de abundância, como viu no filhote. Havia muito poucos clones compartilhados entre os tipos de células neurais ventrais; Isso se encaixa no fato de que a neurogênese ocorre anteriormente neste compartimento. Alguns clones foram compartilhados no tubo neural dorsal, mas apenas entre outros neurônios do mesmo tipo. A única exceção foram os neurônios DI4 e DI5, que ainda compartilhavam a grande maioria dos códigos de barras, o que significa que, no momento da infecção, a decisão de se tornar DI4 ou DI5 ainda não havia sido tomada. Esta parece ser a mais recente decisão de linhagem de qualquer neurônio na medula espinhal. Por que isso pode ser importante? Giulia especula que sua proliferação como progenitores pode ajudar a garantir que a proporção last de DI4: DI5 seja equilibrada, pois existem doenças que podem surgir de um desequilíbrio entre esses dois neurônios.
A hipótese de Giulia é que existem dois grupos diferentes de progenitores na medula espinhal dorsal, que dá origem a neurônios DI4 e um que mantém progenitores com potencial bi-fadado. A sequência temporal ainda não está clara; Giulia especula que os diferentes grupos de progenitores podem amadurecer em neurônios a taxas diferentes ou começar a amadurecer em momentos diferentes, resultando em uma proporção aproximada de 1: 1. No momento, não há dados para mostrar o que acontece entre o estágio 28 dominante do DI4 e a restauração do equilíbrio no estágio 31, portanto, não é possível provar quando ou como essa mudança acontece. Atualmente, Giulia está trabalhando para ajustar um modelo aos seus dados, a fim de testar essa hipótese, além de complementar seus dados de sequenciamento com imagens ao vivo para preencher as lacunas temporais.
Fique ligado para mais entrevistas de pôsteres em breve!
Referências:
Holguera, I., Desplan, C., 2018. Especificação neuronal no espaço e no tempo. Science 362, 176-180. https://doi.org/10.1126/science.aas9435
Lai, HC, Seal, RP, Johnson, JE, 2016. Fazendo sentido com o desenvolvimento somatossensorial da medula espinhal. Desenvolvimento 143, 3434-3448. https://doi.org/10.1242/dev.139592
Le Dréau, G., Martí, E., 2012. Padrões dorsal-ventrais do tubo neural: uma história de três sinais. Dev Neurobiol 72, 1471-1481. https://doi.org/10.1002/dneu.22015
Leber, S., Breedlove, S., Sanes, J., 1990. Linhagem, arranjo e morte de motoneurônios relacionados clonalmente na medula espinhal de galinho. J Neurosci 10, 2451-2462. https://doi.org/10.1523/jneurosci.10-07-02451.1990
Leber, SM, SANes, JR, 1991. Análise de linhagem com um retrovírus recombinante: aplicação aos neurônios motores da espinha espinhal. ADV Neurol 56, 27-36.
Sagner, A., Briscoe, J., 2019. Estabelecendo a diversidade neuronal na medula espinhal: um tempo e um lugar. Desenvolvimento 146, dev182154. https://doi.org/10.1242/dev.182154
Weinreb, C., Rodriguez-Fraticelli, A., Camargo, FD, Klein, AM, 2020. O rastreamento da linhagem nos vínculos de paisagens transcricionais indicam para o destino durante a diferenciação. Science 367, EAAW3381. https://doi.org/10.1126/science.aaw3381


 (Sem classificações ainda)
(Sem classificações ainda)




