Em seu artigo recente, Maia-Gil e colegas explorou se e como as propriedades nucleares podem influenciar o posicionamento nuclear in vivo. Seu trabalho revelou que, no neuroepitélio de peixe -zebra de densamente embalado, a deformabilidade nuclear facilita a migração nuclear apical (Maia-Gil et al. 2024). Aqui, eles compartilham a ciência e as aventuras que levaram ao desenvolvimento deste projeto.
O que já period conhecido?
O laboratório Norden tem sido focado em entender a biologia celular e tecidual por trás do desenvolvimento da retina do peixe -zebra há 1,5 décadas até agora. A retina se desenvolve a partir de um neuroepitélio pseudostratificado, composto por uma única camada densamente compactada de células altamente alongadas. Entre outros tópicos, o laboratório está investigando uma marca registrada de neuroepitélia pseudostratificada que é migração nuclear apical antes da mitose. Esse fenômeno é caracterizado por um movimento rápido e direcionado dos núcleos para a superfície apical do tecido. No início deste projeto, já sabíamos:
- Por que Os núcleos migram apicamente: seu posicionamento apical antes da divisão celular garante a integridade do tecido (Strzyz et al. 2015).
- Quando Essa migração ocorre: durante a fase G2 do ciclo celular (Leung et al. 2011).
- Como Movimento de núcleos: usando um mecanismo dependente de actina (Norden et al. 2009 e Yanakieva et al. 2019).
A grande questão: como passar pela multidão … e chegar ao bar?
Uma noite, enquanto o laboratório estava fora para uma reunião social, nos encontramos enfrentando um bar lotado e eu estava lutando para obter minha bebida favorita – Porto Tónico. Determinado a chegar ao barman, começamos a debater maneiras diferentes de navegar pela multidão de maneira rápida e eficiente. No meio de muitas idéias criativas (e impraticáveis), alguém sugeriu brincando: “E se pudéssemos deformar e espremer a multidão – assim como os núcleos durante a migração apical?”
Esta ideia de inchaço levantou uma nova pergunta: A deformabilidade nuclear facilita a migração nuclear apical no neuroepitélio da retina lotada?
Nossa abordagem: endurecendo núcleos e rastreando seu movimento durante o desenvolvimento de órgãos
Já sabíamos que os núcleos retinianos do peixe -zebra são altamente deformáveis e expressam baixos níveis de lamina a/c (Yanakieva et al. 2019), uma proteína do envelope nuclear com nível de expressão que se correlaciona com a rigidez nuclear. Para testar nossa hipótese de que a deformabilidade nuclear ajuda a migração apical, aumentamos a rigidez nuclear usando uma linha transgênica de peixe -zebra gerada anteriormente na qual todos os núcleos superexpressam a lamina A (Amini et al. 2022). Com o suporte essential de nossos colaboradores, usamos microscopia de força atômica (com Elias Barriga e Jaime Espina) e desenvolvemos um modelo mecânico que representa núcleos confinados como gotículas compressíveis (com Anna Erzberger e Roman Belousov) para confirmar que a lamina uma superexpressão liderada para Stiffer, núcleos no neuroepitélio da retina.
A corrida para o lado apical
Com esse conhecimento e nossas ferramentas estabelecidas, usamos microscopia de folha leve para imaginar retinas de peixe-zebra e quantificar a migração nuclear apical in vivo. Nosso objetivo foi responder a várias perguntas importantes:
- Os núcleos mais robustos, lamin a superexpressores, alcançam o lado apical? Sim, mas, em contraste com os núcleos de controle, os núcleos mais rígidos levam duas vezes mais para cobrir distâncias equivalentes. Esse atraso ocorre independentemente de os núcleos circundantes serem rígidos ou normais, sugerindo que a deformabilidade nuclear facilita a migração em um maneira autônoma de células.
- A deformabilidade dos núcleos circundantes afeta a migração apical? Sim! Os núcleos de controle cercados por núcleos mais rígidos também levam mais tempo e mostram um movimento menos direcionado. Isso indica que o propriedades mecânicas do ambiente influenciar a migração nuclear.
- O aumento da rigidez nuclear prejudica a migração apical em um epitélio menos movimentado? Aqui, o efeito foi menos pronunciado. A superexpressão da lamina A no cérebro posterior do peixe -zebra, um neuroepitélio menos movimentado, teve apenas pequenos efeitos na migração nuclear apical. Isso sugere que o O impacto da rigidez nuclear depende da embalagem do tecido.
- A rigidez nuclear afeta outros processos que requerem deformação celular? Sim! As células de controle levaram mais tempo para arredondar antes da mitose quando em um ambiente mais rígido, mostrando que as propriedades nucleares podem influenciar a entrada mitótica em um maneira não-célula-autônoma.
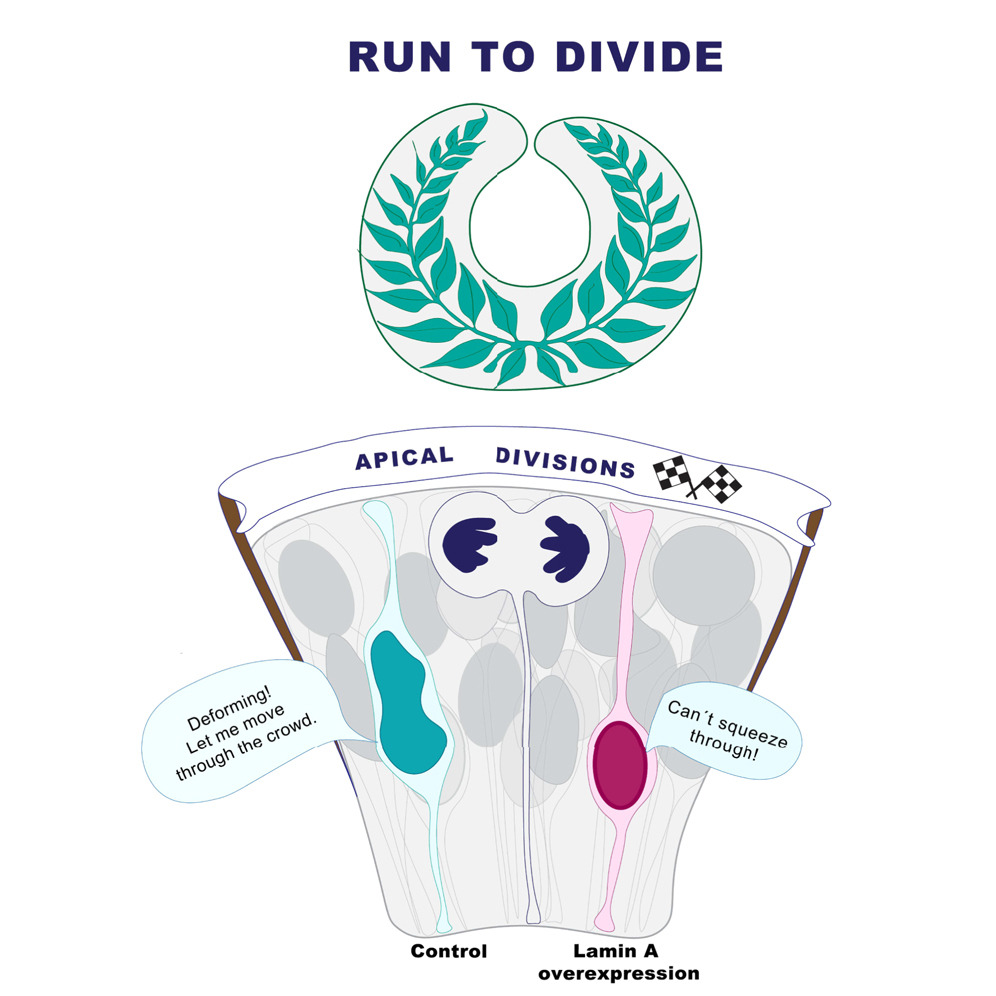
Juntos, esses achados demonstram que as propriedades nucleares influenciam o posicionamento nuclear e a entrada mitótica de maneira dependente do tecido durante o desenvolvimento neuroepitelial.
Um projeto de desenvolvimento pessoal … durante as revisões
Minha barriga estava crescendo, a fadiga estava se instalando e o tempo estava correndo. O electronic mail de revisão chegou com uma lista de tarefas desafiadoras. As prioridades tiveram que ser redefinidas e nossa estratégia ajustada. Precisávamos de mais mãos no banco e tivemos que aprofundar os dados anteriores. O que poderia ter sido uma montanha -russa irregular se transformou em uma aventura científica bem -sucedida e gratificante. Sou grato por ter sido cercado por cientistas destacados que também defendem a mulher na ciência. O incentivo deles foi inestimável – não apenas para o sucesso do meu projeto de doutorado, mas também para o desenvolvimento das duas mais bonitas retinas que já vi.
Referências
1. Maia-Gil, M., Gorjão, M., Belousov, R., Espina, Ja, Coelho, J., Gouhier, J., Ramos, Ap, Barriga, Eh, Erzberger, A. e Norden, C, (2024). A deformabilidade nuclear facilita a migração nuclear apical na retina em desenvolvimento de peixe -zebra. Biologia atual 345429-5443.E8. https://doi.org/10.1016/j.cub.2024.10.015.
2. Strzyz, PJ, Lee, Ho, Sidhaye, J., Weber, IP, Leung, LC e Norden, C. (2015). A migração nuclear intervenética é independente do centrossomo e garante a divisão celular apical para manter a integridade do tecido. Célula de desenvolvimento 32203-219. https://doi.org/10.1016/j.devcel.2014.12.001.
3. Leung, L., Klopper, AV, Grill, SW, Harris, WA e Norden, C. (2011). A migração apical dos núcleos durante o G2 é um pré -requisito para todo o movimento nuclear na neuroepitélia do peixe -zebra. Desenvolvimento 1385003–5013. https://doi.org/10.1242/dev.071522.
4. Norden, C., Younger, S., Hyperlink, BA e Harris, WA (2009). A actomiosina é o principal fator da migração nuclear intervenética na retina. Célula 1381195-1208. https://doi.org/10.1016/j.cell.2009.06.032.
5. Yanakieva, I., Erzberger, A., Matejčić, M., Modes, CD e Norden, C. (2019). A morfologia celular e tecidual determina os mecanismos de migração nuclear dependentes de actina na neuroepitélia. Journal of Cell Biology 2183272-3289. https://doi.org/10.1083/jcb.201901077.
6. Amini, R., Bhatnagar, A., Schlüßler, R., Möllmert, S., Guck, J. e Norden, C. (2022). A migração semelhante a amebóide garante a formação correta da camada de células horizontais na retina em desenvolvimento de vertebrados. eLife 11E76408. https://doi.org/10.7554/elife.76408.


 (Sem classificações ainda)
(Sem classificações ainda)




