Ânion radical octafluorocubano – onde fica o elétron additional?
Derek Lowe relata a história(cite)10.1126/science.abq0516(/cite) que o octafluorocubano recentemente sintetizado pode absorver um elétron para formar um ânion radical – um elétron em um cubo. Então pensei que seria divertido calcular exatamente onde esse elétron está!
Um cálculo de ωB97XD/Def2-TZVPPD/SCRF=clorofórmio (DOI: 10.14469/hpc/11090) é realizado no sistema neutro (otimizando sua geometria) e depois no ânion radical na mesma geometria. Cubos de densidade eletrônica complete são avaliados para ambos e então a forma neutra é subtraída do ânion. O resultado é mostrado abaixo (valor de isosuperfície de densidade 0,0025 au; clique na imagem para carregar um modelo 3D giratório da diferença de densidade).
A seguir está a geometria do ânion otimizada para ambas as espécies;
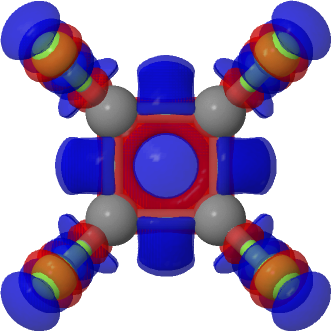
O código de cores é que o azul representa a localização do elétron adicional e o vermelho indica reduzido densidade eletrônica em comparação com o ânion. A seta 1 mostra uma esfera adicional de densidade dentro do cubo – sim, um elétron em um cubo. Mas você provavelmente não teria previsto que a superfície externa do cubo (seta 2) também está cercada por esse elétron e há uma camada de densidade reduzida na superfície interna do cubo. As ligações CF possuem regiões de densidade adicional e densidade reduzida.
Postscript: Perfluorododecaedrano adicionado conforme comentário
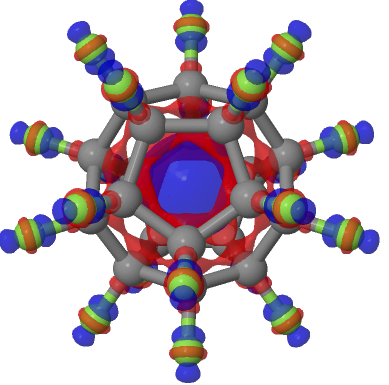
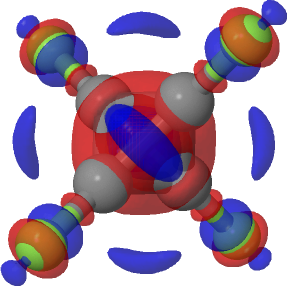
Pós-escrito: Perfluorotetraedro adicionado para completar
Relacionado
Esta entrada foi publicada segunda-feira, 29 de agosto de 2022 às 7h51 e arquivada em Sem categoria. Você pode acompanhar quaisquer respostas a esta entrada através do RSS 2.0 alimentar. Você pode deixe uma respostaou trackback do seu próprio website.






