Nitroarils- Um reagente alternativo menos tóxico para ozonólise: modelagem da etapa last para formar carbonilas.
Às vezes você se depara com uma reação cujo conceito é tão simples que você se pergunta por que demorou tanto para ser realizada na prática. Neste caso, substituindo o ozônio tóxico O3 como usado para fragmentar um alceno em dois compostos carbonílicos (“ozonólise”) por um reagente simples relativamente não tóxico baseado em grupo nitro, ArNO2 em que o átomo central do ozônio é substituído por um grupo N-aril. Conforme relatado por Derek Lowedois grupos publicaram(cite)10.1021/jacs.2c05648(/cite), (cite)10.1038/s41586-022-05211-0(/cite) detalhes de tal reação (Ar = 4-ciano ou 3-CF3,5-NÃO2). Mas existem (pelo menos) dois truques; a primeira é usar fotoexcitação usando LEDs roxos (luz 390nm) para ativar o grupo nitro. A segunda é estabelecer os melhores substituintes aril a serem usados para alcançar rendimentos máximos dos compostos carbonílicos e as melhores condições para alcançar a reação de ciclo-reversão, mostrada abaixo como TS1. Essa etapa requer o aquecimento do ciclo-aduto até ~80° em acetonitrila (aquosa) por qualquer lugar entre 1-48 horas. Aqui, dou uma olhada computacional nessa última etapa, partindo da premissa de que, se tal modelo estiver disponível para esse mecanismo, ele poderá, em princípio, ser usado para otimizar as condições do processo.
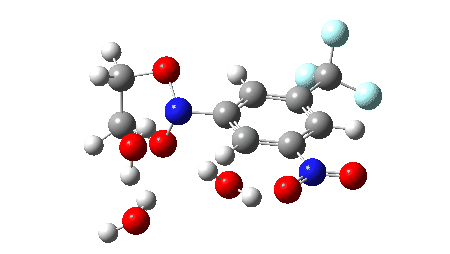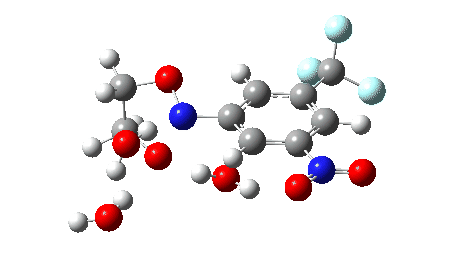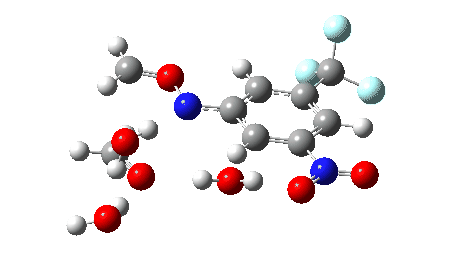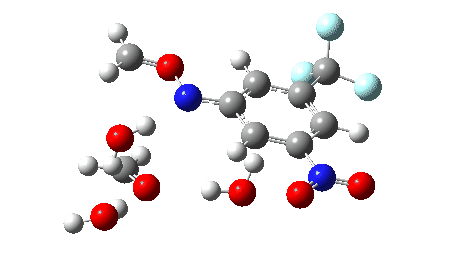
O mecanismo proposto para a investigação em acetonitrila aquosa(cite)10.1038/s41586-022-05211-0(/cite) é mostrado abaixo, envolvendo TS1 (uma reação de cicloreversão pericíclica térmica), TS2 e TS3 envolvendo a intervenção de duas ou três moléculas de água para produzir os compostos carbonílicos e uma aril hidroxilamina (que pode por si só ser um produto valioso). Também foi discutido(cite)10.1038/s41586-022-05211-0(/cite) que um mecanismo alternativo poderia envolver a extrusão de um aril nitreno em vez de uma cicloreversão (mostrada como TS4). Os cálculos utilizam o seguinte método: (U)ωB97XD/Def2-TZVPP/SCRF=acetonitrila. O DOI de dados FAIR para eles é 10.14469/hpc/11269.
Como o processamento ocorre até ~80° em acetonitrila aquosa,(cite)10.1038/s41586-022-05211-0(/cite) a energia livre de ativação que permitiria isso deve ser <~25 kcal/mol.
- O primeiro modelo é uma ciclo-reversão de casca fechada simples, solvatada apenas pelo modelo contínuo, fornecendo uma barreira (para o eteno como substrato) que é um pouco alta para uma reação térmica relativamente fácil.
- Neste nível, a reação de extrusão do nitreno identifica-se como um ponto de sela de segunda ordem com uma energia muito alta, eliminando-a da possibilidade do mecanismo.
- Permitindo que a função de onda tenha algum caráter biradical (TS1 tem
2> antes da aniquilação 0,5534, depois de 0,0858; um biradical puro para o qual os estados singleto e tripleto são iguais em energia teria um valor de 1,00) reduz a energia em modestos 2,5 kcal/mol neste modelo, mas produzindo uma barreira de energia livre um pouco mais realista. - Adicionando 2H2O para o modelo permite TS2 e TS3 ser comparado diretamente com TS1. A barreira cai mais 3,0 ou 4,3 kcal/mol respectivamente para 2 ou 3 águas, e também indica claramente que TS1 é a etapa limitante da taxa. A barreira corresponde a uma reacção que é razoavelmente rápida à temperatura ambiente ou ligeiramente elevada.
| Modelo | ΔG‡ TS1 | ΔG‡ TS2 | ΔG‡ TS3 |
|---|---|---|---|
| Reagentes | 0 | ||
| Casca fechada iônica | 30,0 | – | |
| “TS4” | 73,9 | – | |
| + biradical | 27,5 | – | |
| +biradical + 2H2O | 24,5 | 13.7 | 9.2 |
| +biradical + 3H2O | 23.2 | 12.6 | -1,5 |
| Produtos + 3H2O | -20,4 | ||
Os resultados aqui poderiam ser usados para por exemplo exploração computacional de como a variação no grupo aromático pode afetar a barreira para a cicloreversão.‡ Idealmente, uma versão desta reacção que pudesse operar a temperaturas muito mais baixas melhoraria esta alternativa à utilização de ozono.
‡ O ΔG‡valor para p-CN.3H2O é mais baixo (22,1 kcal/mol vs 23,3 kcal/mol), sugerindo que ocorre mais rapidamente do que o m-CF3,NÃO2 versão. Esta postagem tem DOI: 10.14469/hpc/11319
Relacionado
Etiquetas: Química interessante
Esta entrada foi publicada em sábado, 8 de outubro de 2022 às 8h31 e arquivada em mecanismo de reação. Você pode acompanhar quaisquer respostas a esta entrada através do RSS 2.0 alimentar. Você pode deixe uma respostaou trackback do seu próprio website.






