O tópico do dicarbono, C2já vem sendo discutido aqui há alguns anos. Sem dúvida seria um gás! Este aspecto da espécie veio à tona recentemente(cite)10.1039/D2CP01214F(/cite) quando novos experimentos com um potencial precursor químico do dicarbono, o zwitterion X(+)-C≡C(-), mostraram que diferentes variantes de X(+), como não apenas X=PhI(+), mas também por exemplo X=dibenzotiofenio(+) pareceu gerar uma espécie gasosa, que poderia ser capturada como “C2”Em um experimento de balão conectado sem solvente.
Parte do mistério é que C2 em si é extremamente alta energia espécie, sua dimerização para C4 sendo em torno de 107 kcal/mol exoenergético em energia livre. Agora, cálculos anteriores(cite)10.1039/D1CP02056K(/cite) revelaram que a reação do precursor PhI(+)-C≡C(-) consigo mesmo pode ocorrer em uma by way of de energia relativamente baixa que evita a energia muito alta de C2. O IRC para esta reação é mostrado abaixo, mostrando uma barreira modesta e uma reação muito exotérmica para as espécies PhI(+)-CCCC(-) e IPh.
Aqui chamo sua atenção para um recurso estranho no IRC, na região de -5. Nesta região, efetivamente “C livre4”é formado (a uma energia cerca de 60 kcal/mol menor que a dos reagentes e 167 kcal/mol menor que duas moléculas de C livre2), mas esta espécie é imediatamente capturada por um PhI para formar os produtos finais com uma diminuição adicional na energia de ~20 kcal/mol. Suponhamos, no entanto, no sentido da dinâmica molecular, que alguma proporção deste “C4” poderia seguir uma trajetória diferente e se libertar neste ponto, escapando assim de ser preso pelo PhI? Esta reação geraria então o que novamente é presumivelmente um C gasoso4.
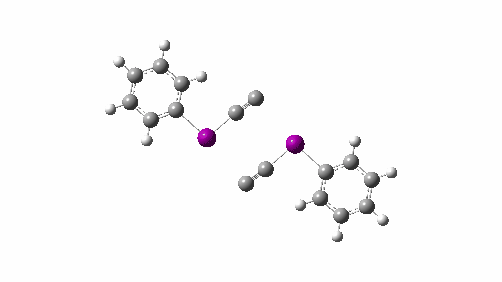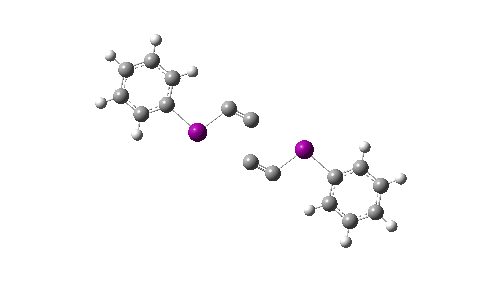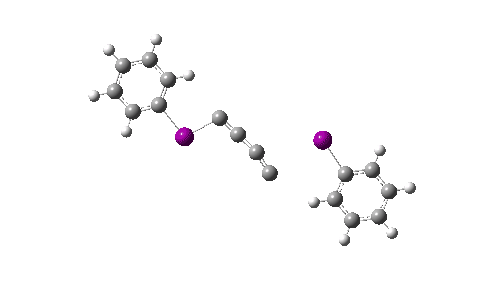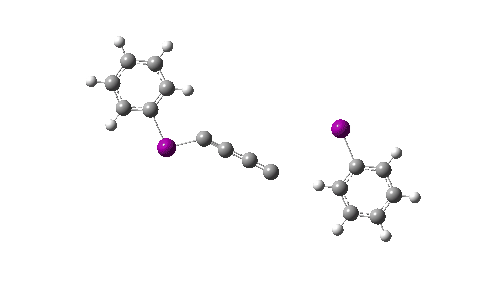
Aqui eu exploro o que pode acontecer a seguir, para responder à questão de saber se C linear4 é estável ou será convertido em outra coisa? O esquema abaixo mostra alguns dos caminhos possíveis, levando à forma bicíclica que desenvolvi discutido anteriormente extensivamente em termos de sua aromatização estabilizadora. Os cálculos são feitos no nível da fase gasosa CCSD(T)/Def2-TZVPPD, permitindo a formação de birradicais (FAIR Knowledge DOI: 10.14469/hpc/11956).
Você pode ver que C4 está em um poço térmico modesto, com uma barreira de energia livre à ciclização de ~22 kcal/mol. Assim gerado a energias relativamente baixas, poderá reter a sua estrutura linear, enquanto que à temperatura ambiente ou superior, provavelmente terminará como espécie aromática bicíclica.
O cálculo principal pode ser a reação de dimerização mostrada acima. A dinâmica molecular mostraria que uma proporção da reação permite o escape de C4? Isso seria dependente da temperatura/pressão? Não estou disposto a tentar esses cálculos, mas as ofertas para fazê-lo serão aceitas com prazer! Mas isso não resolve necessariamente o mistério desta reação, aludida acima.(cite)10.1039/D2CP01214F(/cite) A espécie gasosa aprisionada é C2 em si, C4 de alguma forma, ou mesmo algo totalmente diferente?
Esta postagem tem DOI: 10.14469/hpc/11959
Relacionado
Esta entrada foi publicada terça-feira, 29 de novembro de 2022 às 15h06 e arquivada em mecanismo de reação. Você pode acompanhar quaisquer respostas a esta entrada através do RSS 2.0 alimentar. Você pode deixe uma respostaou trackback do seu próprio web site.





